Recente analyses en studies hebben hoop gewekt om de mensheid te beschermen tegen antibioticaresistentie, die snel een wereldwijde bedreiging aan het worden is.
De ontdekking van antibiotica in het midden van de twintigste eeuw was een belangrijke mijlpaal in de geschiedenis van de geneeskunde, omdat het een wondermiddel was voor veel bacteriële infecties en bacterie-veroorzakende ziekten. Antibiotica werden ooit een "wondermiddel" genoemd en nu zijn antibiotica onmisbaar in zowel de basisgezondheidszorg als geavanceerde medische zorg en technologie, omdat ze de wereld echt hebben veranderd door levens te beschermen en een essentieel onderdeel te zijn van de behandeling van verschillende medische aandoeningen en assistentie bij kritieke chirurgische ingrepen. procedures.
Resistentie tegen antibiotica groeit in hoog tempo
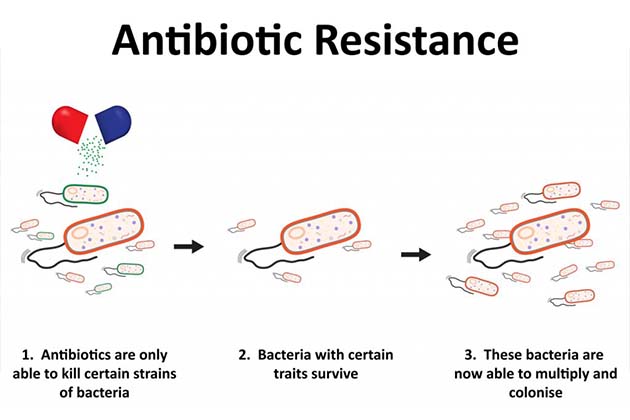
Antibiotica zijn medicijnen die van nature door micro-organismen worden geproduceerd en die stoppen of doden bacteriën van groeien. Het is van cruciaal belang omdat bacteriële infecties de mensheid door de tijd heen hebben geplaagd. Maar ‘resistente’ bacteriën ontwikkelen een verdedigingsmechanisme dat hen beschermt tegen de effecten van antibiotica, terwijl ze voorheen door hen werden gedood. Deze resistente bacteriën zijn dan in staat om eventuele aanvallen van antibiotica te weerstaan en als deze bacteriën ziekteverwekkend zijn, werken standaardbehandelingen niet meer tegen die ziekte, waardoor de infecties voortduren die zich vervolgens gemakkelijk naar anderen kunnen verspreiden. Zo zijn de ‘magische’ antibiotica helaas begonnen te falen of ineffectief te worden, en dit vormt een enorme bedreiging voor het gezondheidszorgsysteem wereldwijd. Het aantal resistente bacteriën veroorzaakt elk jaar al meer dan 500,000 sterfgevallen en erodeert de efficiëntie van antibiotica voor preventie en genezing door een stille moordenaar te zijn, omdat ze in een of andere vorm in bijna 60% van de wereldbevolking voorkomen. Resistentie tegen antibiotica bedreigt ons vermogen om vele ziekten zoals tuberculose, longontsteking te genezen en vooruitgang te boeken op het gebied van operaties, behandeling van kanker enz. Naar schatting zullen tegen 50 ongeveer 2050 miljoen mensen sterven aan antibioticaresistente infecties en de dag zou kunnen komen dat antibiotica niet langer kunnen worden gebruikt voor de behandeling van kritieke infecties zoals ze nu worden gebruikt. Deze kwestie van antibioticaresistentie is nu een belangrijk gezondheidsonderwerp dat dringend moet worden aangepakt voor een betere toekomst, en de medische en wetenschappelijke gemeenschap en de regeringen over de hele wereld nemen verschillende stappen om dit doel te bereiken.
WHO-enquête: het 'post-antibioticumtijdperk'?
Wereldgezondheidsorganisatie (WHO) heeft verklaard: resistentie tegen antibiotica een hoge prioriteit en ernstig gezondheidsprobleem via zijn Global Antimicrobial Resistance Surveillance System (GLASS) dat in oktober 2015 werd gelanceerd. Dit systeem verzamelt, analyseert en deelt gegevens over antibioticaresistentie wereldwijd. Vanaf 2017 hebben 52 landen (25 hoge-inkomens-, 20-middeninkomens- en zeven lage-inkomenslanden) zich ingeschreven voor GLASS. Het is een eerste verslag1 met informatie over antibioticaresistentieniveaus geleverd door 22 landen (een half miljoen deelnemers aan het onderzoek) die een alarmerende groei laten zien - in het algemeen een enorme resistentie van 62 tot 82 procent. Dit initiatief van de WHO heeft tot doel bewustzijn te creëren en te coördineren tussen verschillende landen om dit ernstige probleem op mondiaal niveau aan te pakken.
We hadden antibioticaresistentie kunnen voorkomen en kunnen dat nog steeds
Hoe hebben we deze fase van de mensheid bereikt waarin antibioticaresistentie een wereldwijde bedreiging is geworden? Het antwoord daarop is vrij eenvoudig: we hebben extreem veel antibiotica gebruikt en verkeerd gebruikt. De artsen hebben de afgelopen decennia aan een of elke patiënt overdreven antibiotica voorgeschreven. Ook in veel landen, vooral de ontwikkelingslanden van Azië en Afrika, antibiotica zijn zonder recept verkrijgbaar bij de plaatselijke apotheker en kunnen worden gekocht zonder zelfs maar een doktersrecept. Geschat wordt dat 50 procent van de tijd antibiotica worden voorgeschreven voor virusveroorzakende infecties waar ze in principe geen zin in hebben, omdat het virus zijn levensduur nog steeds zal voltooien (meestal tussen 3-10 dagen), ongeacht of antibiotica worden ingenomen of niet. In feite is het gewoon onjuist en voor velen een mysterie hoe antibiotica (die zich richten op bacteriën) precies enig effect zullen hebben op virussen! De antibiotica zouden 'misschien' sommige symptomen van de virale infectie kunnen verlichten. Zelfs dan blijft dit medisch onethisch. Het juiste advies zou moeten zijn dat, aangezien er voor de meeste virussen geen behandeling beschikbaar is, de infectie gewoon zijn gang moet gaan en dat deze infecties in de toekomst moeten worden voorkomen door strikte hygiëne te volgen en de omgeving schoon te houden. Bovendien worden antibiotica routinematig gebruikt om de landbouwproductie wereldwijd te verbeteren en om als groeisupplement aan vee en voedselproducerende dieren (kip, koe, varken) te voeren. Door dit te doen lopen mensen ook een groot risico om antibioticaresistent in te nemen bacteriën die zich in dat voedsel of die dieren bevinden en die een rigoureuze overdracht van resistente stambacteriën over de grenzen veroorzaken.
Dit scenario wordt verder gecompliceerd door het feit dat er de afgelopen decennia geen nieuwe antibiotica zijn ontwikkeld door farmaceutische bedrijven. De laatste nieuwe antibioticaklasse voor gram-negatieve bacteriën waren de chinolonen die vier decennia geleden werden ontwikkeld. Dus, zoals we er nu voorstaan, kunnen we niet echt aan preventie denken resistentie tegen antibiotica door meer en andere antibiotica toe te voegen, omdat dit de resistentie en overdracht alleen maar compliceert. Veel drug bedrijven hebben erop gewezen dat het ontwikkelen van nieuwe drug is ten eerste erg duur omdat het een lang proces is dat enorme investeringen vereist en de potentiële winst van antibiotica is over het algemeen zo laag dat de bedrijven niet in staat zijn om 'break-even' te maken. Dit wordt vertroebeld door het feit dat er binnen twee jaar na de lancering ergens ter wereld een resistente stam zou ontstaan voor een nieuw antibioticum, aangezien er geen wettelijk kader bestaat om overmatig gebruik van antibiotica aan banden te leggen. Dit klinkt zowel commercieel als medisch niet bepaald hoopgevend en dus is het ontwikkelen van nieuwe antibiotica niet de oplossing om resistentie te voorkomen.
WHO beveelt actieplan aan2 voor het voorkomen van antibioticaresistentie:
a) Beroepsbeoefenaren in de gezondheidszorg en werknemers moeten een zorgvuldige gedetailleerde beoordeling uitvoeren voordat antibiotica aan mens of dier worden voorgeschreven. Een Cochrane-overzicht van verschillende methoden3 gericht op het terugdringen van antibioticamisbruik in elke klinische opzet heeft geconcludeerd dat de '3-dagenvoorschrift'-methode redelijk succesvol was, waarbij de patiënt die lijdt aan een infectie (die niet bacterieel is) wordt overgebracht dat zijn/haar toestand zal verbeteren in 3 dagen, anders kunnen antibiotica worden ingenomen als de symptomen verergeren - wat over het algemeen niet het geval is, aangezien de virale infectie tegen die tijd zijn beloop heeft gehad. b) Het grote publiek moet erop kunnen vertrouwen dat ze vragen stellen wanneer ze antibiotica krijgen voorgeschreven en ze mogen alleen antibiotica gebruiken als ze ervan overtuigd zijn dat het absoluut noodzakelijk is. Ze moeten ook de voorgeschreven dosering voltooien om snelle groei van resistente bacteriestammen te voorkomen. c) Landbouwers en veehouders dienen een gereguleerd, beperkt gebruik van antibiotica te volgen en dit alleen te doen waar het ertoe doet (bijvoorbeeld om een infectie te behandelen). d) Overheden moeten plannen op nationaal niveau opzetten en volgen om antibioticagebruik in te dammen1. Voor ontwikkelde landen en midden- en lage-inkomenslanden moeten op hun behoeften afgestemde kaders worden opgesteld.
Nu het kwaad geschied is: antibioticaresistentie aanpakken
Om te voorkomen dat we ons in een nieuw 'post-antibiotica'-tijdperk begeven en terugkeren naar het pre-penicilline-tijdperk (eerste antibioticum dat ontdekt wordt), vindt er veel onderzoek plaats op dit gebied vol mislukkingen en incidentele successen. Recente meerdere onderzoeken tonen manieren aan om antibioticaresistentie aan te pakken en misschien om te keren. De eerste studie gepubliceerd in Journal of Antimicrobiële Chemotherapie4 laat zien dat wanneer bacteriën resistent worden, is een van de manieren die ze gebruiken om de werking van antibiotica te beperken, door een enzym (een β-lactamase) te produceren dat elk antibioticum vernietigt dat de cel probeert binnen te komen (voor behandeling). Manieren om de werking van dergelijke enzymen te remmen, zouden dus met succes antibioticaresistentie kunnen omkeren. In een tweede daaropvolgende studie van hetzelfde team aan de Universiteit van Bristol, VK, maar in samenwerking met de Universiteit van Oxford, gepubliceerd in: Moleculaire microbiologie5, analyseerden ze de effectiviteit van twee soorten remmers van dergelijke enzymen. Deze remmers (uit de bicyclische boronaatklasse) bleken zeer effectief te zijn tegen een bepaald type antibioticum (aztreonam), zodat het antibioticum in aanwezigheid van deze remmer veel resistente bacteriën kon doden. Twee van dergelijke remmers avibactam en vaborbactam – ondergaan nu klinische proeven en hebben het leven kunnen redden van een persoon die lijdt aan een onbehandelbare infectie. De auteurs zijn erin geslaagd met slechts een bepaald type antibioticum, niettemin heeft hun werk hoop gewekt om het tij van antibioticaresistentie te keren.
In een andere studie gepubliceerd in Wetenschappelijke rapporten6, hebben onderzoekers van de Université de Montréal een nieuwe benadering bedacht om de overdracht van resistentie tussen bacteriën te blokkeren, wat een van de manieren is waarop de antibioticaresistentie zich verspreidt in ziekenhuizen en gezondheidsafdelingen. De genen die verantwoordelijk zijn voor het resistent maken van de bacteriën zijn gecodeerd op plasmiden (een kleine DNA fragment dat onafhankelijk kan repliceren) en deze plasmiden worden overgedragen tussen de bacteriën, waardoor de resistente bacteriën heinde en verre. Onderzoekers screenden een bibliotheek van kleine chemische moleculen die zouden binden aan het eiwit (TraE) dat essentieel is voor deze plasmide-overdracht. De bindingsplaats van de remmer is bekend uit de 3D-moleculaire structuur van het eiwit en men zag dat zodra potentiële remmers aan het eiwit waren gebonden, de overdracht van antibioticaresistente, gendragende plasmiden aanzienlijk was verminderd, wat een mogelijke strategie suggereert voor het beperken en omkeren van antibiotica weerstand. Voor dit soort onderzoek is echter 3D moleculaire structuur van een eiwit is vereist, wat het enigszins beperkend maakt, aangezien veel eiwitten nog structureel moeten worden gekarakteriseerd. Desalniettemin is het idee bemoedigend en zouden dergelijke remmers waarschijnlijk een belangrijke rol kunnen spelen in de dagelijkse gezondheidszorg.
Antibioticaresistentie bedreigt en ondermijnt tientallen jaren van verbeteringen en winsten die zijn gemaakt bij de mens gezondheidszorg en ontwikkeling en de implementatie van dit werk zal een enorme directe impact hebben op het vermogen van mensen om gezond te leven.
***
{U kunt de originele onderzoekspaper lezen door op de DOI-link hieronder in de lijst met geciteerde bron(nen) te klikken}
Bron (nen)
1. WIE. Global antimicrobiële resistentie surveillance systeem (GLASS) rapport. http://www.who.int/glass/resources/publications/early-implementation-report/en/ [Toegang tot 29 januari 2018].
2. WIE. Hoe antibioticaresistentie te stoppen? Hier is een recept van de WHO. http://www.who.int/mediacentre/commentaries/stop-antibiotic-resistance/en/. [Toegang tot 10 februari 2018].
3. Arnold SR. en Straus SE. 2005. Interventies om het voorschrijven van antibiotica in de ambulante zorg te verbeteren.Cochrane Database Syst Rev. 19 (4). https://doi.org/10.1002/14651858.CD003539.pub2
4. Jiménez-Castellanos JC. et al. 2017. Envelopproteoomveranderingen aangedreven door RamA-overproductie in Klebsiella pneumoniae die de verworven β-lactamresistentie verbeteren. Journal of Antimicrobiële Chemotherapie. 73(1) https://doi.org/10.1093/jac/dkx345
5. Calvopiña K. et al.2017. Structurele/mechanistische inzichten in de werkzaamheid van niet-klassieke β-lactamaseremmers tegen extensief resistente klinische isolaten van stenotrophomonasmaltophilia. Moleculaire Microbiologie. 106 (3). https://doi.org/10.1111/mmi.13831
6. Casu B. et al. 2017. Op fragmenten gebaseerde screening identificeert nieuwe doelen voor remmers van conjugatieve overdracht van antimicrobiële resistentie door plasmide pKM101. Wetenschappelijke rapporten. 7 (1). https://doi.org/10.1038/s41598-017-14953-1